Theo nghị định 15/2018/NĐ-CP của chính phủ, từ 1/7/2019 tất cả các cơ sở sản xuất bảo vệ sức khỏe không đạt GMP sẽ không được sản xuất. Vì vậy, giấy chứng nhận GMP là điều kiện bắt buộc để các nhà máy dược phẩm được tiếp tục sản xuất cũng như là tăng độ uy tín của sản phẩm và doanh nghiệp. Vậy chứng nhận GMP là gì? Quy trình chứng nhận GMP như thế nào? Hãy tham khảo bài viết dưới đây.
GMP là gì
GMP (Good Manufacturing Practices) là tiêu chuẩn thực hành sản xuất tốt nhằm đảm bảo điều kiện vệ sinh an toàn cho sản xuất. GMP là một phần cơ bản trong hệ thống quản lý an toàn thực phẩm. Là điều kiện tiến quyết cho việc phát triển hệ thống HACCP và các tiêu chuẩn quản lý an toàn thực phẩm ISO 22000.

GMP là tiêu chuẩn bắt buộc thực hiện đối với các đơn vị sản xuất Thuốc – Thuốc thú y – Hóa Mỹ phẩm – Phân bón
– Thực phẩm chức năng – Phụ gia thực phẩm
GMP đưa ra các yêu cầu:
– Nhà xưởng và trang thiết bị: khu vực nhà xưởng, khu vực chế biến, xử lý thưc phẩm, phương tiện vệ sinh, phương tiện chiếu sang, thông gió, thiết bị và dụng cụ, hệ thống an toàn trong trường hợp khẩn cấp.
– Kiểm soát vệ sinh nhà xưởng làm vệ sinh nhà xưởng, xử lý chất thải, bảo quản hóa chất nguy hại, đồ dùng cá nhân
– Kiểm soát quá trình chế biến: đối với nguyên vật liệu, hoạt động sản xuất.
– Kiểm soát về con người: yêu cầu về sức khỏe, cách ly nguồn lây nhiễm, vệ sinh cá nhân, giáo dục, kiểm soát
– Vận chuyển và bảo quản thành phẩm.
Đối tượng cần chứng nhận GMP
Như đã nói ở trên, GMP được áp dụng trong các lĩnh vực sản xuất, chế biến các sản phẩm yêu cầu điều kiện vệ sinh cao như:
– Thực phẩm
– Dược phẩm,
– Mỹ phẩm,
– Thiết bị y tế.
Trong lĩnh vực thực phẩm, nhà hàng, khách sạn. Cũng rất thích hợp cho việc áp dụng GMP.
Yêu cầu điều kiện về sản xuất thử đối với cơ sở đăng ký kiểm tra lần đầu là:
Cơ sở phải sản xuất ít nhất 03 lô sản phẩm trên dây chuyền đăng ký kiểm tra để thẩm định quy trình sản xuất và các vấn đề liên quan như đánh giá hiệu năng thiết bị sản xuất, các tiện ích phụ trợ, thẩm định quy trình vệ sinh; đánh giá năng lực và sự phù hợp của các hoạt động bảo quản, kiểm nghiệm thuốc đối với dây chuyền đăng ký kiểm tra. Các nội dung này phải thể hiện đầy đủ trong hồ sơ lô sản phẩm.
Lợi ích khi có chứng nhận GMP
Áp dụng tiêu chuẩn GMP ngoài việc đáp ứng yêu cầu của pháp luật thì nó còn đem lại rất nhiều lợi ích cho doanh nghiệp:
– Tiêu chuẩn hóa điều kiện vệ sinh và hoạt động kiểm soát vệ sinh nhà xưởng, con người, sản xuất
– Tạo điều kiện thuận lợi cho việc triển khai HACCP, ISO 22000
– Giảm phần lớn nguy cơ ngộ độc, kiện cáo, phàn nàn của khách hàng
– Tăng cường uy tín, sự tin cậy, sự hài lòng của nhà phân phối, khách hàng.
– Cải thiện hoạt động tổng thể của doanh nghiệp
– Giúp giảm chi phí cho việc tái sản xuất và tiền phạt do sự không tuân thủ quy định giảm và hiệu quả hoạt động tăng.
– Khách hàng, nhân viên, cổ đông, các nhà lãnh đạo và đối thủ cạnh trạnh sẽ ngày càng tôn trọng những tổ chức chứng minh được cam kết của mình về vấn đề an toàn thực phẩm
Quy trình chứng nhận GMP
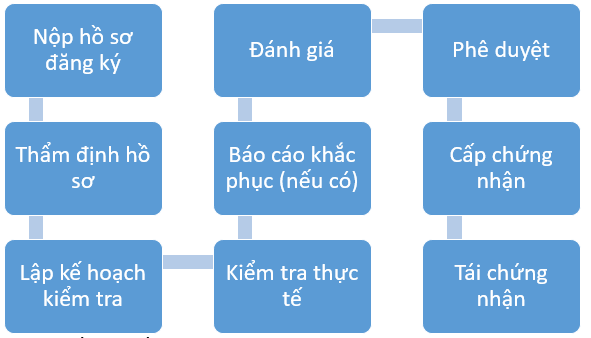
Bước 1: Tiếp nhận hồ sơ đăng ký
Thời gian: 1 ngày.
Doanh nghiệp nộp hồ sơ đến tổ chức chứng nhận để đăng ký chứng nhận GMP
Bước 2: Thẩm định hồ sơ
Thời gian: 1-2 ngày
Đối với hồ sơ đăng ký kiểm tra lần đầu: chuyên gia phải đánh giá sự phù hợp về quy mô và tính hợp lý của việc triển khai tại cơ sở với các dây chuyền cơ sở đăng ký kiểm tra (cấp sạch nhà xưởng; công suất thiết bị, hệ thống; chiều di chuyển của nhân viên, nguyên liệu, bán thành phẩm, thành phẩm; phân công và trình độ của nhân sự chủ chốt;…) và các điểm cần lưu ý trong quá trình kiểm tra (các nội dung chưa phù hợp hoặc nghi ngờ…)
Đối với hồ sơ đăng ký tái kiểm tra: chuyên gia phải xem xét đánh giá kết quả kiểm tra lần trước về mức độ đáp ứng yêu cầu GMP, các thay đổi so với lần kiểm tra trước (các ảnh hưởng của việc thay đổi đến điều kiện môi trường, thiết bị, quy trình,…), báo cáo khắc phục các tồn tại của lần kiểm tra trước (việc thực hiện các tồn tại theo kế hoạch xây dựng được báo cáo gần nhất), các chú ý liên quan đến vi phạm quy định hiện hành về Dược của cơ sở (nếu có): vi phạm về chất lượng thuốc, sản xuất thuốc,….
Bước 3: Lập kế hoạch
Thời gian: 1-2 ngày
Tổ chức chứng nhận lên kế hoạch làm việc với đơn vị đăng ký
Bước 4: Kiểm tra thực tế
Thời gian: 2-5 ngày
Đoàn kiểm tra thực hiện việc kiểm tra thực tế:
– Kiểm tra trực tiếp tại các khu vực sản xuất, kiểm nghiệm, kho bảo quản nguyên liệu, thành phẩm, bao bì, các hệ thống phụ trợ,…
– Kiểm tra rà soát hồ sơ lưu trữ về các hoạt động của cơ sở sản xuất.
Bước 5: Báo cáo khắc phục
Sau buổi kiểm tra, doanh nghiệp sẽ phải khắc phục các lỗi mà chuyên gia ghi nhận, tùy vào từng lỗi mà thời gian khắc phục các đơn vị là khác nhau
Bước 6: Đánh giá báo cáo khắc phục
Sau khi doanh nghiệp đã khắc phục lỗi, tổ chức chứng nhận sẽ đánh giá lại xem đạt hay không
Bước 7: Cấp chứng nhận
Thời gian: 01 ngày
Sau khi báo cáo khắc phục đã được phê duyệt; hồ sơ hoàn thiện thì doanh nghiệp sẽ được cấp chứng nhận GMP
Tổ chức chứng nhận GMP
Công ty Cổ phần Chứng nhận Quốc tế (ICB) được Bộ Khoa học và Công nghệ chỉ định năng lực chứng nhận GMP theo quyết định số 1070/TĐC-HCHQ. ICB cung cấp dịch vụ Tư vấn – Chứng nhận GMP với các chuyên gia có nhiều năm kinh nghiệm trong ngành tiêu chuẩn chất lượng. Cam kết với chi phí và thời gian tiết kiệm nhất.
Ngoài ra, ICB còn có các năng lực chứng nhận khác như ISO 9001, ISO 22000, ISO 14001, ISO 45001, ISO 13485, Vietgap, nông nghiệp hữu cơ,…và hợp chuẩn, hợp quy nhiều sản phẩm khác.
Liên hệ với ICB để được hỗ trợ nhanh nhất: hotline 0913 748 863 – email cert@chungnhanquocte.vn




